Vivant
- Santé, Médecine et Sciences du Vivant
- Biologie & Biochimie
La réparation de l’ADN filmée avec une précision atomique !
- Tweeter
-
-
0 avis :
L’ADN est une molécule fragile qui peut être endommagée par les rayons ultraviolets. Parmi ces lésions, les plus fréquentes sont celles appelées "dimère cyclobutylique de pyrimidine" (ou lésion CPD) : deux bases nucléiques adjacentes se lient entre elles, ce qui casse leur interaction habituelle avec leurs partenaires sur l'autre moitié complémentaire de l'ADN, empêchant les mécanismes de réplication ou de transcription au-delà du point de lésion. Pour réparer ces lésions, l’enzyme photolyase utilise la lumière bleue qu’elle capte, aidée par une ou plusieurs molécules appelées cofacteurs. Toutefois, le mécanisme précis de cette réaction n’avait, jusqu’à aujourd’hui, jamais été observé.
Dans une étude parue dans la revue Science, des scientifiques ont utilisé deux grands instruments de type laser de rayons X à électrons libres (XFEL), le SwissFEL en Suisse et SACLA au Japon, pour visualiser le mécanisme moléculaire de réparation d'un brin d'ADN par l’enzyme photolyase provenant d’un microorganisme. Les outils utilisés leur ont permis d’obtenir un film moléculaire de la réaction entre 100 picosecondes (une picoseconde est à une seconde ce qu'une seconde est à environ 31 689 ans) et 200 microsecondes (une microseconde est à une seconde ce qu'une seconde est à environ 2 ans), à un niveau de détail atomique jamais atteint auparavant.
Le mécanisme ainsi observé se déroule comme suit : dans un premier temps, l’enzyme photolyase équipée de son cofacteur flavine (ici une molécule de FAD) vient se fixer sur l’ADN lésé. Lorsque le cofacteur absorbe un photon de lumière bleue, un électron est transféré très rapidement du cofacteur vers l'ADN, puis les deux liaisons covalentes entre les deux bases adjacentes sont rompues successivement. S’ensuit le réarrangement des différents groupes chimiques impliqués dans la réaction, avec le retour d’un électron vers le cofacteur. Enfin, les deux bases de l'ADN réparées basculent depuis l'intérieur de l’enzyme vers l'intérieur de l'hélice d'ADN, préparant ainsi la dissociation du complexe enzyme/ADN.
L'ensemble des données recueillies dans cette étude constitue un véritable film moléculaire de la séquence complète des événements de la réparation de l’ADN par la photolyase, depuis l'absorption d'un photon lumineux par le cofacteur jusqu'à la dissociation du complexe.
Ces travaux démontrent l’importance des nouvelles technologies mises à disposition de la communauté des biologistes par des grands instruments comme XFEL. Etre capable d’observer comment n’importe quelle enzyme stabilise ses intermédiaires réactionnels offre des perspectives nouvelles pour mieux appréhender ces espèces à durée de vie ultracourte que l’on soupçonne depuis longtemps de jouer un rôle fondamental dans les transformations chimiques indispensables à la vie.
Article rédigé par Georges Simmonds pour RT Flash
Noter cet article :
Vous serez certainement intéressé par ces articles :

Une nouvelle approche thérapeutique pour traiter les cancers du cerveau
Une équipe de chercheurs du célèbre Memorial Sloan-Kettering Cancer Center, à New York, a découvert une molécule, le gliocidin, capable de détruire sélectivement les cellules de glioblastome, un ...
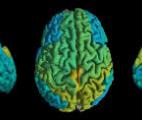
Première carte mondiale des lipides du cerveau humain
Des scientifiques ont découvert que 93 % des lipides du tissu cérébral sont répartis différemment dans la matière blanche et grise, le sous-cortex, les cortex visuel et moteur et le cortex ...
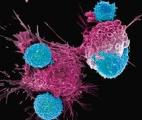
De nouvelles cellules CAR-T permettent de contrôler à la demande le traitement contre le cancer
Des chercheurs de l'Institut Ludwig contre le Cancer (New-York) ont découvert une façon d'activer et de désactiver les cellules CAR-T, pour Chimeric Antigen Receptor en anglais, des lymphocytes T ...
Recommander cet article :
- Nombre de consultations : 0
- Publié dans : Biologie & Biochimie
- Partager :
