Vivant
- Santé, Médecine et Sciences du Vivant
- Biologie & Biochimie
Paludisme et toxoplasmose : découverte d’une protéine clé de l’infection
- Tweeter
-
-
1 avis :
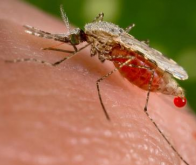
Les mécanismes d’invasion des cellules hôtes par deux parasites de la grande famille des apicomplexes, Toxoplasma gondii et Plasmodium falciparum (respectivement responsables de la toxoplasmose et du paludisme), sont peu à peu élucidés. Maryse Lebrun et son équipe s’y emploient. Ils viennent de découvrir et de décrire une protéine responsable de la libération de facteurs de virulence dans la cellule hôte : RASP2.
Les parasites contiennent notamment deux types de compartiments intracellulaires appelés micronèmes et rhoptries. Ils stockent des protéines impliquées dans l’invasion et la manipulation des cellules et du système immunitaire de l’hôte. Mais la façon dont ces "armes" sont libérées reste un mystère… en particulier pour ce qui concerne celles stockées dans les rhoptries.
Pour en savoir plus, Maryse Lebrun et son équipe ont recherché les protéines présentes à la surface de ces derniers, susceptibles d’être impliquées dans l’expulsion de molécules à travers la membrane cellulaire) des molécules qu'ils contiennent.
Pour ce travail, les chercheurs ont utilisé des banques publiques de données transcriptomiques, permettant de quantifier l’expression des gènes, qui reflètent la production de protéines par un organisme au cours de son cycle de vie. Ils ont regardé quels gènes étaient exprimés et traduits en protéine au cours de la formation de nouvelles rhoptries.
Dans un second temps, ils ont sélectionné les protéines présentes à la fois dans les espèces Toxoplasma et Plasmodium, suspectant qu’un mécanisme comme l’exocytose, aussi déterminant pour la survie du parasite, était vraisemblablement conservé. Enfin, les chercheurs ont regardé si les protéines candidates étaient bien exprimées au pôle apical des rhoptries, c'est-à-dire là où se déroule la libération de leur contenu. C'est ainsi qu'ils ont fini par isoler une famille de protéines qu’ils ont appelées RASP 1, 2 et 3 pour Rhoptry Apical Surface Proteins.
En supprimant sélectivement l’activité de ces protéines dans des parasites en culture, les chercheurs ont constaté que l’absence de RASP1 et 3 n’affectait pas leur fonctionnement. Mais en l’absence de RASP2, ces organismes sont devenus incapables de libérer le contenu des rhoptries et donc d’envahir une cellule hôte, et de survivre. Ils ont alors décortiqué les anomalies fonctionnelles des parasites mutants et analysé la structure de la protéine. Résultat : un domaine de RASP2 peut se lier à deux lipides connus pour être impliqués dans les fusions membranaires, un mécanisme nécessaire à la libération du contenu d’organelles intracellulaires.
Pour les chercheurs, il ne fait donc pas de doute que RASP2 est impliquée dans l’exocytose du contenu des rhoptries, une étape indispensable à l’invasion et la survie intracellulaire de ces parasites. Reste néanmoins à mieux caractériser le fonctionnement et la régulation de RASP2, et à découvrir d’éventuelles molécules partenaires. A terme, Maryse Lebrun espère fournir la description complète des phénomènes d’invasion par ces parasites : cela pourrait ouvrir de nouvelles pistes thérapeutiques contre les maladies dont ils sont responsables.
Article rédigé par Georges Simmonds pour RT Flash
Noter cet article :
Vous serez certainement intéressé par ces articles :
L'édition génomique s'attaque au Sida
C'est un nouvel espoir pour soigner le virus de l’immunodéficience humaine (VIH), une maladie traitable mais incurable qui touche environ 6.000 nouvelles personnes chaque année en France. Une équipe ...

Les statines réduisent la mortalité, même en cas de démence
Une étude de l'université de Berlin montre que l'utilisation de statines est associée à une amélioration de la mortalité chez les personnes âgées résidant en maison de retraite, quel que soit leur ...
Vers un nouveau traitement contre la leucémie aiguë myéloïde
Les docteurs Christophe Ferrand et Marina Deschamps, directeurs de recherche à l'Établissement Français du Sang (EFS) de Besançon, expérimentent une méthode de traitement inédite. Appelé traitement ...
Recommander cet article :
- Nombre de consultations : 0
- Publié dans : Biologie & Biochimie
- Partager :