Vivant
- Santé, Médecine et Sciences du Vivant
- Biologie & Biochimie
Le méthylome, nouvelle carte d’identité épigénétique des cancers
- Tweeter
-
-
2 avis :
Mieux comprendre et traiter le cancer nécessite de décrypter les rouages de cette maladie – ou plutôt de ces maladies, tant il peut prendre des formes multiples. Un moyen en plein développement est de se pencher sur l’ADN. Toutes nos cellules (y compris les cellules tumorales) ont, dans leur noyau, une molécule d’ADN : sorte de long texte où s’enchaînent notamment les gènes et toute l’information génétique qui contribue à nous définir.
Les cancers résultent de modifications de ce texte génétique (on parle de mutations de sa "séquence") survenant dans une cellule, qui peuvent être particulièrement massives et entraîner sa multiplication incontrôlée. Se développe alors une tumeur qui, alors qu’elle grandit et évolue, peut envahir l’organisme.
Les progrès récents des techniques de séquençage "à haut débit" (permettant la lecture rapide du texte génétique) ont permis d’identifier les modifications se cachant derrière de nombreux cancers. Désormais, il est possible de répertorier le "catalogue" de mutations d’une tumeur afin d’établir sa carte d’identité : un atout considérable pour mieux appréhender la nature du cancer en question, ses origines, ses rouages internes et son pronostic. Or, une meilleure compréhension de la maladie contribue au développement de traitements plus efficaces.
Mais l’information génétique ne se situe pas que dans le texte inscrit dans notre ADN… Un second niveau de codage, dit "épigénétique", a été identifié, dont l’étude s’est développée ces dernières décennies. L’épigénétique est à la génétique ce que la ponctuation est à une phrase : le sens d’une phrase sera différent selon la présence et la localisation de virgules, tirets ou parenthèses…
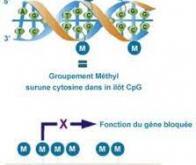
D’un point de vue chimique, nos "virgules génétiques" peuvent prendre la forme d’ajout (ou de retrait) de groupements d’atomes spécifiques – en l’occurrence des méthyls (CH3). La lecture de ce « code » épigénétique permet d’établir un autre type de carte d’identité : le méthylome.
Il y a plusieurs niveaux d’information dans l’ADN : le texte génétique (écrit avec les quatre "lettres" A, T, C et G), qui constitue le génome, et les modifications épigénétiques (notamment les méthylations) qui viennent moduler le message initial. NIH, CC BY-SA
Là encore, son étude fine et sa comparaison avec des méthylomes de cellules saines et tumorales sont riches en informations : si la lecture de la séquence (du texte) génétique renseigne sur les mécanismes de croissance exubérante de la cellule cancéreuse, celle du méthylome précise la nature du cancer et son origine. In fine, le décryptage de ces deux niveaux de données complémentaires contribue à mieux caractériser le cancer et à choisir les traitements anticancéreux les plus adaptés.
Du fait de son coût et du matériel nécessaire pour cartographier la ponctuation de l’ADN, cette technique n’est pour l’heure mise en place que dans certains centres d’oncologie médicale spécialisés. En clinique, c’est surtout en neuro-oncologie (tumeurs du cerveau et de la moelle), pionnière dans le domaine, que son utilisation est la plus aboutie – notamment dans les cas de diagnostic difficile. L’Organisation mondiale de la santé (OMS) recommande d’ailleurs son étude dans le diagnostic de nombreuses tumeurs cérébrales depuis 2021.
Si d’autres types de cancer (sarcomes, développés à partir des os, des muscles, de la graisse…) commencent également à être étudiés par leur méthylome, les résultats sont encore préliminaires.
L'analyse des méthylomes repose sur la bio-informatique et nécessite le développement d’algorithmes (formules de calcul) d’intelligence artificielle (IA). L’idée de base est simple : il faut classer ensemble les tumeurs qui ont la même ponctuation (donc les mêmes variations au niveau épigénétique), à l’instar d’un jeu de 7 familles où le joueur cherche à rassembler les individus d’une même famille.
Une large base de données développée par une équipe de l’Université d’Heidelberg rassemble déjà les profils de méthylation de presque 100 000 tumeurs cérébrales, classées en 80 familles ou sous-familles. En libre accès, elle permet l’envoi de nouvelles données qui sont analysées en ligne gratuitement. L’avantage est double puisque le logiciel propose au médecin pathologiste un classement de la tumeur envoyée, et l’équipe d’Heidelberg enrichit sa base de données, rendant les algorithmes d’IA plus performants – de façon générale, plus un algorithme analyse de tumeurs, plus les classements qu’il propose sont fiables. Cette forme de projet collaboratif international bénéficie ainsi au plus grand nombre : patients, médecins et chercheurs.
Malgré les limites de l’IA, l’analyse du méthylome représente bien un progrès considérable dans le diagnostic des tumeurs cérébrales, notamment de l’enfant – chez qui elles sont beaucoup plus variées que chez l’adulte. En France, les Centres hospitalo-universitaires (CHU) référents en neuro-oncologie s’équipent progressivement afin que, dans les années à venir, une carte d’identité épigénétique puisse être établie pour chaque tumeur cérébrale (en plus de la carte d’identité génétique déjà réalisée).
Article rédigé par Georges Simmonds pour RT Flash
Noter cet article :
Vous serez certainement intéressé par ces articles :

Certains traitements contre le cholestérol diminuent le risque de cancer du foie
Selon une étude de l'Institut National du Cancer Américain, certains médicaments anti-cholestérol diminuent le risque de développer un cancer du foie. Les traitements testés par les auteurs de la ...
Un nouveau traitement contre les tempêtes inflammatoires
Des chercheurs japonais de l'Université d'Osaka viennent de découvrir une nouvelle stratégie thérapeutique contre la tempête de cytokines, un syndrome inflammatoire sévère déclenché par une ...
Sclérose en plaques : un médicament expérimental répare la myéline
Des chercheurs de l’Université du Colorado, en collaboration avec la société Autobahn Therapeutics Inc, dirigée par les professeurs Daniel J. Denman et Ethan G. Hughes, ont montré que la molécule ...
Recommander cet article :
- Nombre de consultations : 0
- Publié dans : Biologie & Biochimie
- Partager :