Vivant
Maladies à prion: des souris infectées se rétablissent pour la première fois
- Tweeter
-
-
0 avis :
Pour la première fois, des animaux de laboratoire ont pu se rétablir d'une maladie neurologique contagieuse à prion, telles la maladie de la vache folle et sa forme humaine, le nouveau variant du Creutzfeldt-Jakob, selon des chercheurs britanniques. Leurs travaux, publiés dans la revue américaine Science, apportent une lueur d'espoir en montrant qu'on peut se rétablir - au moins chez la souris - de ces maladies qui sont actuellement de véritables sentences de mort. Aucun traitement ne guérit ces maladies (Creutzfeldt-Jakob classique ou son nouveau variant, la forme humaine de la maladie de la vache folle, tremblante du mouton, dépérissement chronique du cerf), qui donnent à la cervelle des allures d'éponge. Toutes sont caractérisées par la transformation d'une protéine prion naturellement présente dans le cerveau en une forme anormale. Les auteurs avancent qu'un intermédiaire toxique pendant la conversion des prions à l'intérieur des neurones pourrait être la cause ultime des maladies à prion. "Sur le plan de la recherche thérapeutique, ces travaux suggèrent qu'on se tromperait de cible et qu'il faudrait non pas s'attaquer à la forme anormale mais à la forme normale de la protéine prion" pour tenter d'enrayer la maladie, indique le Pr Jean-Philippe Deslys, expert de ces maladies à prion (France). John Collinge et Giovanna Mallucci (Institut de neurologie de Londres) ont créé des souris mutantes pour débarrasser leurs neurones des prions normaux, afin de vérifier si cela pouvait influer sur le cours de la maladie, qui leur est inoculée. La diminution de prions normaux dans les neurones de ces souris modifiées "a empêché la progression de la maladie et permis aux rongeurs infectés une longue survie", affirment-ils. Elle s'est accompagnée, alors que leur cervelle se trouvait envahie par le prion pathologique (mais pas encore dans les neurones), d'une disparition des premières lésions de spongiose qu'on croyait irréversible, "tout en prévenant la perte des neurones et la progression de la maladie clinique", notent les auteurs. Pour parvenir à ce résultat, l'astuce a consisté à neutraliser l'action d'une enzyme (la "Cre recombinase"), mais de façon à ce que ses effets n'interviennent qu'après la 12e semaine de vie des animaux. Avant cet âge, la protéine normale est présente dans les neurones des souris transgéniques. Peu après leur naissance, les chercheurs ont contaminé (avec une souche de tremblante) les souriceaux permettant ainsi au prion anormal de se propager dans le système nerveux central. Vers l'âge de douze semaines, alors que les souris ne manifestaient pas de symptômes de la maladie, leur cervelle présentait déjà des trous d'éponge, mais le prion pathologique ne s'était pas encore infiltré dans les neurones, selon Science. Ce stade pourrait correspondre au tout début de la maladie chez l'homme, marqué par de subtiles modifications intellectuelles et motrices qui ne peuvent être mises en évidence chez des souris. A ce moment, intervient la modification génétique apportée par les chercheurs: la commande (le gène) de la fabrique de la protéine normale dans les neurones est éteinte. Les neurones ont beau être cernés par des hordes de prions neurotoxiques continuant à s'accumuler dans d'autres cellules du cerveau, ils n'en sont pas affectés. Plus d'un an après - ce qui est très long rapporté à la vie humaine - ces souris "vivent une vie normale", selon Science. Les souris ayant servi de comparaison ont toutes succombé après avoir été contaminées.
Science : http://sciencenow.sciencemag.org/
Noter cet article :
Vous serez certainement intéressé par ces articles :

La solution robotique pour remplacer la valve aortique trouvée par une équipe d'ingénieurs azuréens
Positionner une nouvelle valve aortique avec plus de précision et de façon totalement sécurisée grâce à l’assistance d’un robot : la société française de dispositifs médicaux spécialisée dans le ...
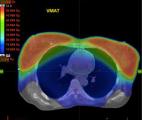
Cancer du sein : une radiothérapie de trois semaines au lieu de cinq donne des résultats aussi efficaces
Une étude va changer la donne pour des dizaines de milliers de femmes atteintes d'un cancer du sein. Elle a été présentée au congrès de cancérologie de l'ESMO (Société européenne d'oncologie ...

Identifier les réactions cliniques des patients à travers leurs yeux fermés
Une nouvelle technologie de l'Université de Tel-Aviv va permettre, pour la première fois au monde, d'identifier les changements de la taille de la pupille et de la direction du regard du patient à ...
Recommander cet article :
- Nombre de consultations : 79
- Publié dans : Médecine
- Partager :