Vivant
- Santé, Médecine et Sciences du Vivant
- Biologie & Biochimie
Des gènes bactériens pour soigner l’arythmie cardiaque
- Tweeter
-
-
0 avis :
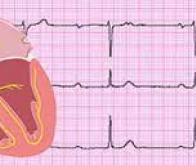
Des bioingénieurs de l’Université de Duke (Caroline du Nord) ont réussi, en utilisant des gènes bactériens modifiés, à exciter les cellules cardiaques chez des souris modèles d’arythmie. Ces travaux illustrent les avancées de ces thérapies géniques minimalement invasives et très ciblées. L’équipe de Durham rappelle que les arythmies cardiaques surviennent lorsque les cellules du muscle cardiaque ne transmettent plus uniformément les signaux électriques qui induisent le pompage du sang de manière cohérente et régulière. La nouvelle thérapie génique à base de gènes bactériens modifiés qui codent pour les canaux ioniques sodium - qui transmettent les charges électriques dans la cellule - apparaît ici prometteuse pour traiter une grande variété de troubles cardiaques « électriques ». Les ingénieurs de la Duke apportent ici une première preuve de concept en montrant, chez la souris modèle d’arythmie, que la nouvelle thérapie génique induit bien les cellules du muscle cardiaque à s'activer électriquement.
Les canaux ioniques sodium sont des protéines dans les membranes externes des cellules électriquement excitables, telles que les cellules cardiaques ou cérébrales, qui transmettent des charges électriques dans la cellule. Dans le cœur, ces canaux indiquent aux cellules musculaires quand se contracter et transmettent l'instruction afin que l'organe pompe le sang telle une unité cohésive. Cependant, les cellules cardiaques endommagées, que ce soit par une maladie ou un traumatisme, perdent souvent tout ou partie de leur capacité à transmettre ces signaux et à se joindre à cet effort collectif.
En délivrant des gènes qui codent pour les canaux ioniques sodium dans les cellules musculaires cardiaques, les chercheurs renforcent la production de canaux ioniques dans les cellules malades, ce qui contribue à rétablir leur activité. Chez la souris, la thérapie génique permet bien d'améliorer la capacité collective des cellules musculaires cardiaques à initier et à propager l'activité électrique et donc la capacité du muscle cardiaque à pomper. « Ce qui est extrêmement difficile à accomplir avec des médicaments ou d'autres thérapies », relève l’auteur principal, Nenad Bursac, professeur de génie biomédical à la Duke. De plus, les effets de cette thérapie génique délivrée aux cellules musculaires cardiaques persistent pendant une longue période, ce qui suggère une solution efficace et durable pour les patients souffrant d’arythmie cardiaque.
Chez les mammifères, les gènes des canaux sodiques sont très volumineux et trop grands pour tenir dans les virus actuellement utilisés comme vecteurs dans les thérapies géniques chez l'Homme. La solution adoptée pour contourner le problème est d’utiliser des gènes plus petits qui codent pour des canaux ioniques sodium similaires dans les bactéries. Si ces gènes bactériens sont différents de leurs homologues humains, l'évolution a conservé de nombreuses similitudes dans la conception des canaux. En faisant muter ces gènes bactériens, il est possible qu’ils deviennent actifs dans les cellules humaines.
in vitro, les chercheurs montrent que ces gènes modifiés ne pénètrent que dans les cellules musculaires actives du cœur dans les oreillettes et les ventricules et fabriquent des protéines tout en flottant librement dans la cellule, en utilisant la machinerie biochimique existante ; de précédentes recherches menées sur cette approche de délivrance de gènes viraux avaient déjà confirmé que les gènes transplantés restent actifs pendant de nombreuses années ; ici, in vitro, la thérapie améliore suffisamment l'excitabilité électrique des cellules cardiaques, pour prévenir les anomalies humaines telles que les arythmies ; enfin, in vivo chez la souris, les canaux ioniques sodium sont bien actifs dans le cœur, montrant des tendances vers une excitabilité améliorée.
Article rédigé par Georges Simmonds pour RT Flash
Noter cet article :
Vous serez certainement intéressé par ces articles :
Découverte d'une cause fondamentale du lupus
Des chercheurs américains viennent de découvrir comment le lupus érythémateux, ou systémique, affecte le système immunitaire. « Les manifestations du lupus peuvent être défigurantes, et même ...

Détecter le manque de sommeil par une prise de sang
Une technologie innovante réussit désormais à identifier une personne qui a été privée de sommeil pendant 24 heures. Ce test sanguin repose sur une combinaison de biomarqueurs présents dans le sang ...
Des cellules souches dopées au glucose pour combattre l’arthrose
Des scientifiques de l'UNIGE ont découvert comment accroître la durée de vie de cellules souches injectées dans le cartilage pour faciliter la régénération de tissus endommagés par l’arthrose. ...
Recommander cet article :
- Nombre de consultations : 0
- Publié dans : Biologie & Biochimie
- Partager :