Vivant
- Santé, Médecine et Sciences du Vivant
- Biologie & Biochimie
Comment diriger la croissance des vaisseaux sanguins
- Tweeter
-
-
0 avis :
Les cellules, qu’elles se trouvent dans le corps ou dans des tissus développés en laboratoire, interagissent constamment avec la matrice extracellulaire (MEC), un réseau moléculaire extrêmement complexe qui fournit un support structurel aux cellules. Jusqu’à récemment, les scientifiques avaient supposé que ces interactions étaient principalement biochimiques.
Mais les chercheurs ont maintenant compris que des interactions mécaniques, comme, par exemple, la capacité des cellules à détecter diverses propriétés de la MEC et à y réagir, jouent également un rôle important dans le développement et le fonctionnement des cellules.
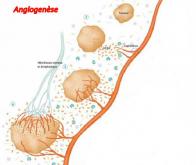
L’un des défis scientifiques de la production de tissus biologiques artificiels destinés à la transplantation est qu’ils doivent contenir un réseau de vaisseaux sanguins pour assurer un apport constant en oxygène et en nutriments aux tissus. L’ordre directionnel de ce réseau est essentiel à l’intégration et à la survie de l’implant. En d’autres termes, les vaisseaux sanguins doivent s’organiser dans le même sens.
Dans le laboratoire du Professeur Levenberg, au Technion, une plate-forme conçue pour améliorer la production de tissus et l’auto-organisation pour la transplantation des tissus a été développée. Cette technologie repose sur des échafaudages polymériques tridimensionnels. Des cellules biologiques essentielles au développement des vaisseaux sanguins sont développées sur ces échafaudages de polymères, ce qui a permis à l’équipe de constater que les forces mécaniques avaient une forte influence sur les propriétés de ces réseaux de vaisseaux sanguins, et en particulier le rôle joué par les directions dans lesquelles ils se développaient.
En 2016, le Professeur Levenberg et le Docteur Rosenfeld, alors doctorante dans son laboratoire, ont montré comment un système d’étirement original, qui appliquait des forces de traction au tissu artificiel, affectait les processus biologiques dans les cellules, notamment la différenciation, la forme, la migration, et l’organisation dans les structures, ainsi que la géométrie du tissu émergent, sa maturité et sa stabilité. Cette étude antérieure a également montré que les forces de traction agissant sur le tissu au cours du développement favorisent la croissance des vaisseaux sanguins avec un ordre directionnel bien défini.
La nouvelle étude, menée par les groupes du Professeur Levenberg (Technion) et du Professeur Eran Bouchbinder (Institut Weizmann), a permis la mise en place d’un protocole permettant de générer de manière contrôlée des tissus synthétiques optimaux, présentant notamment des réseaux riches et stables dans lesquels les vaisseaux sanguins ont un ordre directionnel bien défini. Les chercheurs pensent que ces résultats contribueront à améliorer la possibilité de concevoir des tissus permettant une transplantation réussie chez le patient.
Article rédigé par Georges Simmonds pour RT Flash
Noter cet article :
Vous serez certainement intéressé par ces articles :
Cancer du pancréas : une découverte majeure ouvre la voie à de nouveaux traitements
Avec près de 16 000 cas en France en 2023, le cancer du pancréas est le 6e en termes de fréquence. Pourtant, avec une incidence en augmentation, on estime que ce cancer sera la 2e cause de mortalité ...
AVC : des chercheurs français découvrent une nouvelle piste de traitement très prometteuse
Des chercheurs de l’Inserm de Caen travaillent sur une nouvelle piste visant à repérer et détruire les caillots de sang responsables des AVC. Cette équipe a synthétisé des particules baptisées ...
Une avancée majeure dans la prise en charge du cancer de la vessie
Une étude britannique a montré que le durvalumab, molécule commercialisée par le laboratoire AstraZeneca sous le nom Imfinzi, pourrait bien améliorer considérablement le traitement de ce cancer ...
Recommander cet article :
- Nombre de consultations : 0
- Publié dans : Biologie & Biochimie
- Partager :