Vivant
- Santé, Médecine et Sciences du Vivant
- Biologie & Biochimie
Comment certaines bactéries capturent des gènes de résistance aux antibiotiques dans leur environnement…
- Tweeter
-
-
1 avis :
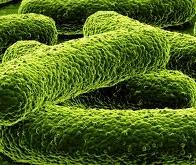
La bactérie Acinetobacter baumannii est responsable d’infections opportunistes (infections causées par des germes habituellement peu pathogènes mais qui provoquent des infections chez les personnes ayant un système immunitaire déficient) et parfois nosocomiales (acquises à l’hôpital). Les infections à A. baumannii ne sont pas très fréquentes mais très difficilement traitables. On observe même des cas de résistance aux antibiotiques de dernier recours, à large spectre, appelés carbapénèmes.
La résistance à plusieurs antibiotiques (multirésistance), lorsqu’elle concerne les carbapénèmes, a conduit l’OMS à classer les souches d’A. baumannii comme des souches prioritaires à étudier pour la recherche de nouveaux antibiotiques. Depuis une décennie, plusieurs analyses de génomes (ADN) de souches multirésistantes d’A. baumannii indiquaient que les gènes de résistance, parfois nombreux, pouvaient être acquis à partir d’autres bactéries de la même espèce voire d’espèces différentes. Le phénomène biologique à l’origine de ces événements de transfert de gènes restait à déterminer. L’étude co-portée par Maria-Halima Laaberki, maître de conférences à VetAgro Sup, et Xavier Charpentier, directeur de recherche à l’Inserm, chef d'équipe au Centre international de recherche en infectiologie de Lyon (CIRI, CNRS/École normale supérieure de Lyon/INSERM/Université Claude Bernard Lyon 1), révèle les conditions dans lesquelles ces événements de transfert se produisent. En effet, ils démontrent qu’une bactérie sensible à un antibiotique est capable en moins de 4 heures d'acquérir les résistances d'une bactérie voisine, dont la résistance aux carbapénèmes.
Ce transfert actif, appelé transformation naturelle (découvert en 1928 par Frederick Griffith chez le pneumocoque et, depuis, chez de nombreuses bactéries), se produit chez la bactérie réceptrice, qui est capable de capter et d'incorporer dans son génome l'ADN des bactéries voisines. Les unités de recherche impliquées sont le Centre international de recherche en infectiologie (CIRI, CNRS/École normale supérieure de Lyon/INSERM/Université Claude Bernard Lyon 1), le Laboratoire de biométrie et biologie évolutive (LBBE, CNRS/VetAgro Sup/ Université Claude Bernard Lyon 1) et Chrono-environnement (CE, CNRS/Université Franche-Comté).
Ce transfert est extrêmement efficace et obtenu à partir d'infimes quantités d'ADN naturellement libérées par les bactéries résistantes voisines. Pour obtenir ces résultats, l’équipe de recherche a mis en œuvre des techniques de génétique bactérienne conventionnelles et basées sur le séquençage de génomes. Cette dernière approche, utilisée ici comme une méthode de cartographie des événements de transfert, a permis de révéler que cette bactérie est capable d’acquérir plus de 80 gènes lors d’un seul événement de transfert.
En quelques heures, A. baumannii peut ainsi modifier plus de 3 % de son génome, lui conférant la capacité de résister à de nombreuses classes d’antibiotiques. Ces résultats permettent de mieux comprendre comment ce pathogène accumule la résistance aux antibiotiques. En lien direct avec les problématiques de santé publique, l’équipe poursuit actuellement ses recherches et travaille à déterminer dans quel milieu cette résistance est acquise et comment anticiper l’apparition de nouvelles résistances.
Article rédigé par Georges Simmonds pour RT Flash
Noter cet article :
Vous serez certainement intéressé par ces articles :

Des chercheurs révèlent un lien inattendu entre fibres alimentaires et cancer du sang
Des chercheurs du réputé Memorial Sloan Kettering Cancer Center (MSK) de New York ont montré qu'un régime alimentaire riche en fibres et à base de plantes pouvait significativement retarder la ...

Des anticorps synthétiques plus faciles à produire
Les anticorps monoclonaux sont essentiels à la recherche biomédicale et aux traitements contre le cancer en raison de leur action ciblée. Ces molécules fabriquées en laboratoire agissent comme les ...
Un nouvel outil de séquençage ADN rapide pour identifier rapidement les bactéries résistantes aux antibiotiques
Les infections bactériennes résistantes aux antibiotiques sont devenues un problème critique pour les hôpitaux du monde entier. Chaque année, ces infections difficiles à traiter causent des dizaines ...
Recommander cet article :
- Nombre de consultations : 0
- Publié dans : Biologie & Biochimie
- Partager :
kalyl
10/07/2024Among Us Online offers an engaging and often hilarious multiplayer experience.