Vivant
- Santé, Médecine et Sciences du Vivant
- Biologie & Biochimie
Des cellules CAR-T améliorées pour détruire plus efficacement lez cellules cancéreuses
- Tweeter
-
-
1 avis :
Des chercheurs de l'EPFL, dirigés par le Professeur Li Tang, ont développé une thérapie innovante, par cellules CAR-T, qui élimine systématiquement les tumeurs cancéreuses chez les souris. Dans le cadre d’essais cliniques en cours, cette thérapie semble engendrer une rémission complète chez les onze patients traités, soit un taux de réussite de 100 %. Les résultats de l’étude de laboratoire laissent notamment entrevoir l’efficacité de la thérapie sur le long terme et le caractère plus rapide et moins onéreux de sa préparation par rapport aux méthodes actuelles.
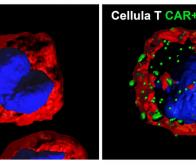
En substance, la thérapie par cellules CAR-T consiste à modifier des lymphocytes T pour cibler et éliminer les cellules cancéreuses. Ces cellules T modifiées, qui constituent une réelle innovation par rapport aux traitements actuels, sont équipées de récepteurs antigéniques chimériques (CAR) capables de reconnaître les cellules cancéreuses et de s’y accrocher. « Nous avons amélioré la thérapie par cellules CAR-T en concevant une cellule immunitaire renforcée, plus robuste, particulièrement efficace pour cibler et éliminer les cellules tumorales », explique Li Tang. La commercialisation du traitement est dans le viseur de la start-up Leman Biotech, cofondée par le professeur Tang et Yugang Guo, coauteur de la publication. La société a déjà réuni d’importants capitaux lors de ses premières levées de fonds.
Les thérapies conventionnelles par cellules CAR-T, par ailleurs efficaces sur les cancers hématologiques, font face à des difficultés contre les tumeurs solides : les cellules s’épuisent et ne parviennent finalement pas à éradiquer le cancer. Les recherches audacieuses menées par le professeur Tang ouvrent de nouvelles perspectives pour ces immunothérapies innovantes. En effet, il a mis au point des cellules CAR-T sécrétant de l’IL-10, une molécule qui est absorbée par les cellules T modifiées. En d’autres termes, la cellule est conçue pour produire son propre remède afin de rester viable dans un environnement tumoral hostile.
Il est intéressant de noter que l’IL-10 est habituellement considérée comme un immunosuppresseur. Mais au lieu de l’utiliser à cette fin, le professeur Tang et son équipe ont tiré parti de ses capacités uniques de renforcement métabolique. Cette innovation, qui permet de booster le métabolisme des cellules CAR-T, fonctionne immédiatement sur les tumeurs existantes et semble empêcher la réapparition de nouvelles tumeurs.
Même après leur réinjection dans les souris, les cellules tumorales n’ont pas réussi à s’installer ou à présenter une quelconque malignité, ce qui montre bien l’efficacité du traitement sur le long terme : le système immunitaire reste réactif et parvient à neutraliser efficacement toute nouvelle menace de récidive. « Les résultats obtenus dans mon laboratoire sont très encourageants », affirme Li Tang. « Nous sommes persuadés que cette technologie est capable de sauver des vies, comme elle l’a déjà fait pour les 12 patients ayant participé à notre étude ».
Même si les thérapies actuelles par cellules CAR-T se sont avérées efficaces et que différentes options de traitement sont aujourd’hui disponibles pour la leucémie et d’autres cancers liquides, celles-ci restent extrêmement onéreuses : le coût d’un seul traitement dépasse les 500 000 dollars. À l’inverse, le coût associé de cette future thérapie pourrait être bien moins élevé, car cinq pour cent de la dose normale suffisent à susciter une guérison complète. « Une petite quantité de sang prélevée sur le patient suffit à produire assez de cellules pour mettre au point une thérapie par cellules CAR-T à l’aide de notre technologie », précise le chercheur. « Il est alors possible de lui réinjecter ces cellules dès le lendemain. Ce nouveau traitement, bien plus abordable et plus rapide à produire, permettrait en fin de compte de sauver plus de vies », souligne le Professeur Li Tang.
Noter cet article :
Vous serez certainement intéressé par ces articles :

Une nouvelle immunothérapie efficace contre le cancer des os
Chaque année, en France, 100 à 150 patients sont touchés par l’ostéosarcome, selon le centre Gustave Roussy. Il s’agit d’un cancer des os qui survient généralement au niveau du genou, à l’extrémité ...
Le corps fabriquerait ses propres antibiotiques
Des chercheurs israéliens dirigés par Yifat Merbl, professeure à l’Institut des sciences Weizmann, se sont intéressés au protéasome, un système de gestion des déchets des cellules humaines. Le rôle ...

Des résultats cliniques positifs pour un nouveau vaccin thérapeutique contre le cancer du poumon
La société liégeoise PDCline Pharma a enregistré de bons résultats cliniques en phase I/II avec son vaccin thérapeutique contre le cancer du poumon. Elle va lever des fonds pour passer à l'étape ...
Recommander cet article :
- Nombre de consultations : 0
- Publié dans : Biologie & Biochimie
- Partager :