Vivant
- Santé, Médecine et Sciences du Vivant
- Biologie & Biochimie
Bloquer les capteurs de Spike pour désarmer le Covid…
- Tweeter
-
-
1 avis :
C’est une première mondiale très prometteuse ! Des scientifiques UCLouvain sont parvenus à identifier et à actionner la clé qui permet au virus du covid de s’attaquer aux cellules. Malgré l’efficacité des campagnes de vaccination partout à travers le monde, la menace que représente la COVID-19 n’est pas encore totalement éloignée. Premièrement, nous ne sommes pas à l’abri de l’apparition d’un nouveau variant du SARS-CoV-2 contre lequel les vaccins actuels ne seraient pas efficaces. Ensuite, l’efficacité des vaccins sur le long terme reste inconnue. Enfin, des cas d’infection aiguë sont toujours rapportés. Or, à ce jour, aucun traitement efficace n’existe.
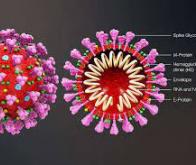
Afin de développer un antiviral empêchant l’infection, il est d’abord nécessaire de comprendre les mécanismes précis (au niveau moléculaire) utilisés par le virus pour infecter une cellule. C’est la tâche à laquelle s’attèle depuis 2 ans l’équipe de David Alsteens, chercheur à l’Institut des sciences et technologies biomoléculaires de l’UCLouvain. Ces chercheurs ont investigué l’interaction entre les acides sialiques (AS), sortes de résidus de sucre présents à la surface des cellules, et la protéine spike (S) du SARS-CoV-2 (à l’aide de la microscopie à force atomique). L’objectif ? Elucider son rôle dans le processus d’infection.
Toutes les cellules sont décorées avec des résidus de sucres. Le job de ces sucres ? Favoriser la reconnaissance des cellules, ce qui permet notamment aux virus d’identifier plus facilement leurs cibles. Mais également, faciliter leur point d’accroche pour leur permettre d’entrer dans leur cellule hôte et d’ainsi initier leur infection.
Les chercheurs UCLouvain ont mis en évidence une variante de ces sucres (9-O-acétylés) interagissant de manière plus forte avec la protéine S que les autres sucres. En clair, ils ont trouvé le trousseau de clés qui permet aux virus d’ouvrir la porte des cellules. Pourquoi un trousseau ? Le virus est composé d’une série de protéines spike, sortes de ventouses qui lui permettent de s’accrocher à la cellule et in fine d’entrer. Plus le virus trouve de clés, meilleure sera l’interaction avec la cellule et plus grand s’ouvrira la porte. D’où l’importance de trouver comment le virus parvient à démultiplier les clés d’entrée.
C’est là qu’intervient la 2e découverte des chercheurs UCLouvain : ils ont décidé de prendre le virus à son propre piège, en l’empêchant de s’accrocher à sa cellule hôte. Comment ? En bloquant les points d’accroche de la protéine S et donc en supprimant toute interaction avec la surface cellulaire. Comme si un cadenas bloquait la serrure de la porte d’entrée de la cellule. Pour ce faire, une des conditions est que l’interaction entre le virus et l’agent bloquant soit plus forte que celle entre le virus et la cellule.
Dans ce cas précis, les scientifiques ont démontré que des structures multivalentes (ou glycoclusters) présentant de multiples acides sialiques 9-O-acétylés à leur surface (la fameuse variante de sucre mise à jour par l’équipe UCLouvain) sont capables de bloquer aussi bien la liaison que l’infection du SARS-CoV-2. Si le virus ne s’attache pas aux cellules, il ne sait plus entrer et donc il meurt (temps de vie 1h à 5h). Grâce à ce blocage, on empêche l’infection.
Dans le cadre de la pandémie de COVID-19, les différents vaccins se sont attaqués principalement aux mutations du SARS-CoV-2, mais pas au virus dans son ensemble. Cette découverte UCLouvain a l’avantage d’agir sur le virus, indépendamment des mutations. La suite ? L’équipe UCLouvain va réaliser des tests sur la souris afin d’appliquer ce blocage des liaisons du virus et observer si cela fonctionne sur l’organisme. Les résultats ne devraient pas tarder et devraient permettre de mettre au point un antiviral à partir de ces sucres, administré par aérosol, en cas d’infection ou de contact à risque.
Article rédigé par Georges Simmonds pour RT Flash
Noter cet article :
Vous serez certainement intéressé par ces articles :
Une nouvelle technique accélère le criblage des molécules d'ADN
L’étude du comportement des molécules d’ADN nous aide à mieux comprendre les maladies génétiques et à concevoir de meilleurs médicaments. Jusqu’à présent, l’examen des molécules d’ADN une par une ...

Les aliments ultra-transformés augmentent les risques de déclin cognitif et d'AVC
Une étude américaine réalisée par des chercheurs du Massachusetts General Hospital à Boston montre que la consommation d'aliments ultra-transformés peut augmenter le risque d'accident vasculaire ...

Les édulcorants augmenteraient le risque de maladies cardiovasculaires
Des chercheurs chinois de l'université de Shandong se sont intéressés plus particulièrement aux mécanismes d'action de l'aspartame, l’un des substituts du sucre les plus courants. Les chercheurs ont ...
Recommander cet article :
- Nombre de consultations : 0
- Publié dans : Biologie & Biochimie
- Partager :